尨巕椡僔僗僥儉尋媶奐敪帠嬈媦傃尨巕椡婎慴婎斦愴棯尋媶僀僯僔傾僥傿僽丂惉壥曬崘夛帒椏廤
曻幩慄桿敪僾儕儞夘嵼宆嵶朎娫忣曬揱払偺夝柧偲偑傫帯椕傊偺墳梡
乮尋媶戙昞幰乯寧杮岝弐 栻妛晹栻妛壢
乮尋媶奐敪婜娫乯暯惉俀侽擭搙乣俀侾擭搙
侾丏尋媶奐敪偺攚宨偲偹傜偄
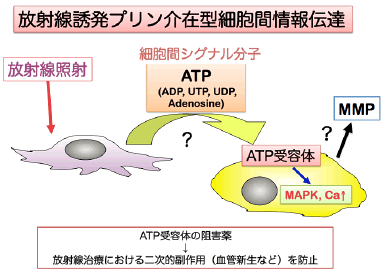
丂曻幩慄徠幩偼丄偑傫嵶朎傪嶦柵偡傞桳岠側帯椕庤抜偲偟偰棙梡偝傟偰偄傞丅偟偐偟丄曻幩慄徠幩偵傛偭偰惗偒巆偭偨偑傫嵶朎偺埆惈壔傗徠幩椞堟嬤朤偺寣娗怴惗槾恑偼丄曻幩慄帯椕帪偺梊屻埆壔偺尨場偲側傞偑丄偦偺尨場偼姰慡偵柧傜偐偲側偭偰偄側偄丅偦偺偨傔丄偙偺傛偆側曻幩慄偺擇師揑塭嬁偺婡彉傪柧傜偐偵偟丄偦偺嶌梡傪慾奞偡傞栻嵻偑奐敪偱偒傟偽曻幩慄偵傛傞偑傫帯椕傪傛傝岠棪揑偵偡傞偙偲偑壜擻偲側傞丅
丂嬤擭丄曻幩慄徠幩偵傛傞惗暔嶌梡傪専摙偡傞嵺丄捈愙徠幩偝傟偨嵶朎偺傒側傜偢徠幩嵶朎廃埻偺旕徠幩嵶朎偵偍偄偰傕曻幩慄徠幩偺塭嬁偑偱傞偙偲偑柧傜偐偲側傝丄僶僀僗僞儞僟乕岠壥偲屇偽傟偰偄傞丅僶僀僗僞儞僟乕岠壥偼丄壗傜偐偺場巕偑徠幩嵶朎偐傜旕徠幩嵶朎傊偲忣曬傪揱偊偰偄傞偲峫偊傜傟傞偑丄偦偺慡梕偼枹偩柧傜偐偵偝傟偰偍傜偢偦偺夝柧偑朷傑傟偰偄傞丅偙偺僶僀僗僞儞僟乕岠壥偼曻幩慄偺擇師揑塭嬁偵娭梌偟偰偄傞壜擻惈偑崅偄偨傔丄僶僀僗僞儞僟乕岠壥偺儊僇僯僘儉傪柧傜偐偵偟曻幩慄偵傛傞擇師揑塭嬁偺堦抂傪夝柧偡傞偙偲偼廳梫側壽戣偱偁傞丅偦偙偱杮尋媶偱偼丄巋寖偵墳偠偰嵶朎奜偵曻弌偝傟傞ATP偲嵶朎枌忋偵敪尰偡傞ATP庴梕懱乮P2庴梕懱乯偵拝栚偟丄僶僀僗僞儞僟乕岠壥偺怴婯儊僇僯僘儉傪専摙偡傞丅
丂ATP偼丄嵶朎撪偵偍偄偰僄僱儖僊乕嫙梌懱偲偟偰摥偒丄嵶朎奜偱偼捠忢旕忢偵掅偄擹搙偵曐偨傟偰偄傞丅偟偐偟丄嵶朎奜偐傜偺僗僩儗僗巋寖偵傛傝ATP偼梕堈偵嵶朎奜傊偲曻弌偝傟丄嵶朎枌忋偵敪尰偡傞ATP摿堎揑庴梕懱乮P2庴梕懱乯傪妶惈壔偝偣傞偙偲偱丄條乆側惗棟嶌梡傪敪尰偝偣傞嵶朎娫忣曬揱払暔幙偲偟偰偺婡擻傪壥偨偡丅偟偐偟側偑傜丄偙傟傑偱偵曻幩慄偵傛傞惗暔塭嬁偵偍偗傞ATP庴梕懱偺娭梌偵偮偄偰専摙偟偨曬崘偼側偄丅
丂偦偙偱丄杮帠嬈偱偼丄曻幩慄偑傫帯椕帪偺暃嶌梡乮寣娗怴惗槾恑丒偑傫怹弫擻槾恑乯傪慾奞偡傞栻嵻偺奐敪傪栚揑偲偟偰丄曻幩慄擇師揑塭嬁傊偺ATP庴梕懱偺娭梌偵偮偄偰埲壓偺尋媶崁栚偺専摙傪峴偆丅
(1) 曻幩慄偵傛傞惗暔塭嬁偵偍偗傞ATP庴梕懱偺娭梌
(2) 偑傫嵶朎偐傜偺曻幩慄桿敪matrix metalloproteinase (MMP)曻弌偵偍偗傞ATP庴梕懱偺娭梌
(3) 儅僂僗偱偺曻幩慄桿敪寣娗怴惗槾恑偵懳偡傞ATP庴梕懱慾奞栻偺岠壥
俀丏尋媶奐敪惉壥
亂尋媶崁栚1亃僸僩昞旂HaCaT嵶朎偵偍偄偰兞慄徠幩乮0.1-1.0 Gy乯偵傛傝嵶朎偐傜ATP偑曻弌偝傟傞偙偲偑柧傜偐偵側偭偨丅偙偺ATP曻弌偼丄嵶朎忈奞偱偼側偔傾僯僆儞僠儍僱儖側偳傪夘偟偰偄傞偙偲偑帵嵈偝傟偨丅兞慄徠幩偵傛傝extracellular signal regulated protein kinase1/2乮ERK1/2乯偑妶惈壔偡傞丅偙偺ERK1/2妶惈壔偼丄嵶朎奜僰僋儗僆僠僪暘夝峺慺傗P2Y6庴梕懱慾奞栻偺張抲偵傛傝梷惂偝傟偨丅偙傟傜偺寢壥偐傜丄兞慄徠幩偵傛偭偰ATP側偳偺僰僋儗僆僠僪偑曻弌偝傟丄曻弌偝傟偨嵶朎奜ATP偵傛傝P2Y6庴梕懱傪娷傓ATP庴梕懱偑妶惈壔偟丄ERK1/2偑妶惈壔偟偰偄傞儊僇僯僘儉偑帵嵈偝傟偨丅
亂尋媶崁栚2亃偑傫嵶朎乮儅僂僗B16儊儔僲乕儅乯偵偍偄偰兞慄徠幩偵傛傝ATP偺曻弌偑擣傔傜傟偨丅傑偨丄徠幩偵傛傝MMP偺曻弌偑擣傔傜傟偨丅徠幩偵傛傞MMP曻弌偼P2X7庴梕懱慾奞栻偵傛偭偰慾奞偝傟偨偨傔丄偑傫嵶朎偐傜偺MMP偺曻弌偵P2X7庴梕懱妶惈壔偑娭梌偡傞偙偲偑帵嵈偝傟偨丅尋媶崁栚1, 2偺寢壥偵傛傝丄曻幩慄惗暔塭嬁偵偍偗傞ATP庴梕懱妶惈壔偺娭梌偑in vitro偵偍偄偰帵偝傟偨丅
亂尋媶崁栚3亃曻幩慄偵傛傞擇師揑塭嬁偵偍偗傞ATP庴梕懱偺娭梌傪in vivo偺儌僨儖偵偍偄偰専摙偟偨丅擇師揑塭嬁偲偟偰偼曻幩慄桿敪寣娗怴惗偵拝栚偟専摙偟偨丅儅僂僗偺戝戁摦柆傪寢鉌偡傞屻巿嫊寣儌僨儖傪梡偄偰専摙偟偨丅嫊寣庤弍屻2廡娫丄慡恎偺寣棳検傪儗乕僓乕僪僢僾儔乕幃寣棳夋憸夝愅憰抲偵傛傝夋憸夝愅偟偨丅兞慄乮0.5 Gy乯徠幩偵傛偭偰傛傝憗婜偵屻巿嫊寣晹埵偺寣棳検偑夞暅偟丄曻幩慄偵傛傞寣娗怴惗槾恑偑帵偝傟偨丅P2X7庴梕懱慾奞栻傪徠幩慜偵搳梌偟偨偲偙傠丄兞慄偵傛傞寣娗怴惗槾恑偑梷惂偝傟傞偙偲偑帵偝傟偨丅偙偺寢壥偼丄偑傫曻幩慄帯椕帪偵偍偄偰丄徠幩慜偵P2X7庴梕懱慾奞栻傪搳梌偟偰偍偔偙偲偱曻幩慄偵傛傞寣娗怴惗槾恑傪梷惂偡傞偙偲偑偱偒丄傛傝岠棪傛偔曻幩慄帯椕傪峴偆偙偲偑弌棃傞壜擻惈傪帵偟偨丅崱夞偺尋媶偱偼寣娗怴惗偵拝栚偟偨偑丄傎偐偵傕曻幩慄偺擇師揑塭嬁偱偁傞偑傫嵶朎偺揮堏懀恑岠壥側偳偝傑偞傑側尰徾偵嵶朎奜ATP偲ATP庴梕懱偺妶惈壔偑娭梌偟偰偄傞壜擻惈偑峫偊傜傟傞丅
俁丏崱屻偺揥朷
丂杮尋媶偵傛偭偰丄曻幩慄桿敪僾儕儞夘嵼宆嵶朎娫忣曬揱払乮Radiation-induced purinergic signaling乯偲偄偆怴偨側曻幩慄惗暔妛偺僷儔僟僀儉偑帵嵈偝傟偨丅嬤擭丄徠幩嵶朎偐傜偝傑偞傑側場巕偑嵶朎奜偵曻弌偝傟偰廃埻偺嵶朎偵嶌梡傪媦傏偡僶僀僗僞儞僟乕岠壥偑拲栚偝傟偰偄傞丅ATP偼偳偺嵶朎偵傕懚嵼偡傞偨傔丄偝傑偞傑側嵶朎偵偍偗傞曻幩慄惗暔嶌梡乮僶僀僗僞儞僟乕岠壥娷傓乯偵娭梌偟偰偄傞壜擻惈偑崅偄丅崱屻偝傑偞傑側曻幩慄惗暔嶌梡偵偍偄偰ATP庴梕懱偺娭梌傪専摙偡傞偙偲偵傛傝丄曻幩慄偺怴偨側嶌梡婡彉偑柧傜偐偵側偭偰偔傞偲峫偊傜傟丄戝偒側攇媦岠壥偑婜懸偱偒傞丅
丂傑偨丄曻幩慄惗暔塭嬁偵偍偗傞暃師揑塭嬁傪傛傝惓妋偵攃埇偡傞偙偲偑偱偒傞傛偆偵側傟偽丄傛傝岠壥揑側曻幩慄帯椕傪幚尰偡傞偙偲偑壜擻偲側傞丅ATP庴梕懱慾奞栻偺徠幩慜搳梌偼丄懡偔偺曻幩慄帯椕偵偍偄偰墳梡偺壜擻惈偑偁傞偨傔丄曻幩慄帯椕姵幰偺惗懚棪岦忋傗偑傫嵞敪丒揮堏杊巭偵偍偄偰峷專偑婜懸偱偒傞丅杮尋媶偱偼曻幩慄徠幩偵傛傞寣娗怴惗槾恑嶌梡偵拲栚偟偨偑丄崱屻偼丄曻幩慄掞峈惈丄偑傫埆惈壔丄墛徢丄慄堐壔傊偺娭梌側偳丄偝傑偞傑側曻幩慄惗暔嶌梡偵偍偗傞ATP庴梕懱偺娭梌傪専摙偟丄傛傝椙偄曻幩慄偑傫帯椕傪幚尰偡傞偨傔偺怴栻偺憂弌偵峷專偟偰偄偒偨偄丅
